INJEKSJONSVÆSKE, oppløsning i ferdigfylt penn 7,5 mg, 10 mg, 12,5 mg, 15 mg, 17,5 mg, 20 mg, 22,5 mg, 25 mg og 30 mg: Hver ferdigfylte penn inneh.: Metotreksatdinatrium tilsv. metotreksat 7,5 mg, resp. 10 mg, 12,5 mg, 15 mg, 17,5 mg, 20 mg, 22,5 mg, 25 mg og 30 mg, natriumklorid, natriumhydroksid og saltsyre (til pH-justering), vann til injeksjonsvæsker.
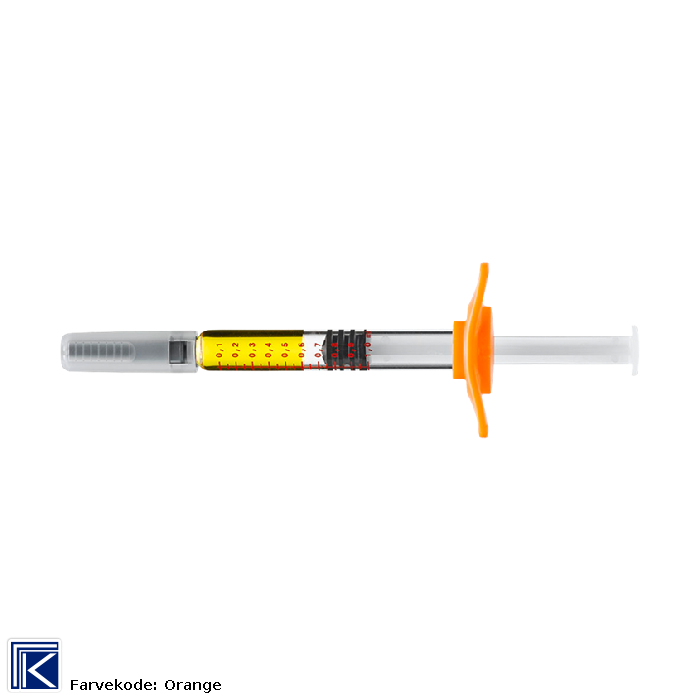
INJEKSJONSVÆSKE, oppløsning i ferdigfylt sprøyte 7,5 mg, 10 mg, 12,5 mg, 15 mg, 17,5 mg, 20 mg, 22,5 mg, 25 mg og 30 mg: Hver ferdigfylte sprøyte inneh.: Metotreksatdinatrium tilsv. metotreksat 7,5 mg, resp. 10 mg, 12,5 mg, 15 mg, 17,5 mg, 20 mg, 22,5 mg, 25 mg og 30 mg, natriumklorid, natriumhydroksid til pH-justering, vann til injeksjonsvæsker.
Indikasjoner
Injeksjonsvæske i ferdigfylt penn:- Aktiv revmatoid artritt hos voksne.
- Polyartrittiske former av alvorlig, aktiv, juvenil, idiopatisk artritt, hvor respons på NSAID ikke har vært adekvat.
- Moderat til alvorlig psoriasis hos voksne som er kandidater for systemisk behandling, samt kraftig psoriasisartritt hos voksne.
- Mild til moderat Crohns sykdom, enten alene eller i kombinasjon med kortikosteroider, hos voksne som ikke reagerer på behandling eller som er intolerante overfor tiopuriner.
- Aktiv revmatoid artritt hos voksne.
- Forskjellige former av alvorlig, aktiv, juvenil, idiopatisk artritt, hvor respons på NSAID ikke har vært adekvat.
- Alvorlig vedvarende, invalidiserende psoriasis, som ikke gir adekvat respons på andre former av behandling, f.eks. fototerapi, PUVA og retinoider, samt kraftig psoriasisartritt hos voksne.
- Mild til moderat Crohns sykdom, enten alene eller i kombinasjon med kortikosteroider, hos voksne som ikke reagerer på behandling eller som er intolerante overfor tiopuriner.
Dosering
Viktig advarsel om dosering av Metex (metotreksat): Ved behandling av revmatoid artritt, juvenil idiopatisk artritt, psoriasis, psoriasisartritt og Crohns sykdom, skal Metex kun brukes 1 gang i uken. Feildosering kan føre til alvorlige bivirkninger, inkl. dødsfall. Les følgende avsnitt svært nøye. Metotreksat bør kun forskrives av lege med ekspertise innen bruk av metotreksat og grundig forståelse av risikoene ved metotreksatbehandling. Pasienten som selv skal sette metotreksat, må få opplæring og trening i korrekt injeksjonsteknikk. Den første injeksjonen med Metex bør utføres under direkte tilsyn av lege. Injiseres s.c. 1 gang pr. uke. Pasienten skal uttrykkelig informeres om at administreringen kun skjer 1 gang i uken. Det anbefales å velge en fast ukedag. Eliminasjonen av metotreksat er redusert hos pasienter med et 3. distribusjonsområde (ascites, pleuraeffusjoner). Slike pasienter må overvåkes spesielt nøye mtp. toksisitet, og krever dosereduksjon eller i enkelte tilfeller seponering av metotreksat.- Nedsatt leverfunksjon: Må administreres med stor forsiktighet, hvis overhodet, ved signifikant aktiv eller tidligere leversykdom, spesielt som følge av alkohol. Bruk av metotreksat er kontraindisert ved bilirubin >5 mg/dl (85,5 μmol/liter).
- Nedsatt nyrefunksjon: Bør brukes med forsiktighet ved nedsatt nyrefunksjon. Dosen bør justeres som følger:
Kreatininclearance (ml/minutt)
Dose
≥60
100%
30-59
50%
<30
Skal ikke brukes
- Eldre: Dosereduksjon skal vurderes pga. redusert lever- og nyrefunksjon samt lavere folatreserver. Pasienter med et 3. distribusjonsområde (pleuraeffusjoner, ascites): Siden halveringstiden kan forlenges med 4 ganger, kan dosereduksjon eller i enkelte tilfeller seponering, være nødvendig.
Penn med gjennomsiktig beskyttelseshette og blått kanyledeksel, med 2-trinns automatisk injeksjonsenhet (YpsoMate-penn): |
|
|---|---|
Kun til s.c. engangsbruk. Det beste stedet for injeksjonen er: Øvre del av låret. På nedre del av magen, unntatt 5 cm rundt navlen. Rens injeksjonsstedet. Dra den gjennomsiktige beskyttelseshetten rett av. Plasser det blå kanyledekslet uten hette i en 90-graders vinkel mot huden. Det er ikke nødvendig å lage en hudfold. Start injeksjonen ved å trykke pennen helt ned (du hører et klikk som angir at injeksjonen starter). Fortsett å holde pennen ned mot huden for å fullføre injeksjonen til du hører et nytt klikk (kort tid etter det første klikket) eller til den blå stempelstangen har sluttet å bevege seg og fyller inspeksjonsvinduet eller til det har gått 5 sekunder. Fjern pennen fra huden i samme 90-graders vinkel. Det blå kanyledekslet går tilbake og låses automatisk på plass over kanylen. Se for øvrig pakningsvedlegget for instruksjoner. |
|
Ferdigfylt sprøyte: |
|
|---|---|
Kun til engangsbruk, gis s.c. Se pakningsvedlegget for instruksjoner. Administreringen skal normalt utføres av rutinert helsepersonell. Hvis den kliniske situasjonen tillater det, kan behandlende lege i visse tilfeller delegere den s.c. administreringen til pasienten selv. I slike tilfeller kreves følgende detaljerte instruksjon fra legen: Det beste stedet for injeksjonen er: Øverst på lårene. På magen, bortsett fra rundt navlen. Rengjør området på og rundt valgt injeksjonssted med såpe og vann eller desinfeksjonsmiddel. Trekk beskyttelseshetten av plast rett av. Ta tak i en hudfold på injeksjonsstedet, og klem forsiktig sammen. Hold fast i hudfolden til sprøyten er fjernet fra huden etter injeksjonen. Skyv nålen helt inn i huden i 90-graders vinkel. Skyv stempelet sakte ned og injiser væsken under huden. Fjern sprøyten fra huden i samme vinkel, på 90 grader. Se for øvrig pakningsvedlegget. |
|
Kontraindikasjoner
Overfølsomhet for innholdsstoffene. Alvorlig nedsatt leverfunksjon. Alkoholmisbruk. Alvorlig nedsatt nyrefunksjon (ClCR <30 ml/minutt). Underliggende bloddyskrasi, f.eks. benmargshypoplasi, leukopeni, trombocytopeni eller signifikant anemi. Alvorlige, akutte eller kroniske infeksjoner, f.eks. tuberkulose, hiv eller andre immunsviktsyndromer, sår i munnhulen og kjent aktiv gastrointestinal ulcussykdom. Graviditet og amming. Samtidig vaksinering med levende vaksiner.Forsiktighetsregler
Pasienten må få tydelig beskjed om at behandlingen kun skal administreres 1 gang i uken, ikke hver dag. Pasienten skal være under passende overvåkning, slik at tegn på ev. toksiske effekter eller bivirkninger kan oppdages og vurderes med minimal forsinkelse. Behandlingen bør derfor kun initieres og overvåkes av lege med kunnskap og erfaring innen antimetabolittbehandling. Pga. muligheten for alvorlige eller til og med fatale toksiske reaksjoner, må legen fortelle pasienten om alle relaterte risikoer og anbefalte sikkerhetstiltak. Fullstendig blodtelling med differensialtelling og telling av trombocytter, testing for leverenzymer, bilirubin, serumalbumin, røntgen thorax og nyrefunksjonstester, anbefales før metotreksatbehandling startes eller gjenopptas etter en hvileperiode. Ved klinisk indikasjon må tuberkulose og hepatitt ekskluderes. Følgende undersøkelser og sikkerhetstiltak anbefales i løpet av behandlingen: Testene i tabellen under skal utføres 1 gang i uken de 2 første ukene, deretter hver 2. uke den neste måneden, etter dette, avhengig av leukocyttallet og pasientens stabilitet, minst 1 gang i måneden i løpet av de neste 6 månedene og minst hver 3. måned etterpå. Det skal også vurderes økt overvåkningsfrekvens ved økning av dosen. Særlig skal eldre pasienter undersøkes for tidlige tegn på toksisitet i korte intervaller.1. |
Undersøkelse av munn og hals for slimhinneendringer. |
2. |
Fullstendig blodtelling med differensialtelling og telling av trombocytter. Enhver betydelig nedgang av antall leukocytter eller trombocytter indiserer umiddelbar seponering og egnet støttende behandling. Pasienten skal oppfordres til å rapportere alle tegn/symptomer som kan tyde på infeksjon. Pasienter som samtidig benytter hematotoksiske legemidler (f.eks. leflunomid) bør overvåkes nøye med blodcelletelling og telling av trombocytter. |
3. |
Leverfunksjonstester: Behandling bør ikke startes, eller bør seponeres, ved vedvarende/signifikante unormale leverfunksjonstester, andre ikke-invasive undersøkelser av leverfibrose eller leverbiopsier. Midlertidig økte transaminaser på 2-3 × ULN med hyppighet på 13-20% er sett. Vedvarende økning av leverenzymer og/eller reduksjon i serumalbumin kan være indikasjon på alvorlig hepatotoksisitet. Ved vedvarende økning av leverenzymer skal dosereduksjon/seponering vurderes. Histologiske endringer, fibrose og, i sjeldnere tilfeller, levercirrhose, kan forekomme uten foregående unormale leverfunksjonstester. Det finnes tilfeller av cirrhose med normale transaminaser. Ikke-invasive diagnostiske metoder for overvåkning av leverstatus skal derfor overveies i tillegg til leverfunksjonstester. Leverbiopsi må overveies individuelt mht. komorbiditeter, anamnese og risiko forbundet med biopsi. Risikofaktorer for hepatotoksisitet inkluderer høyt tidligere alkoholinntak, vedvarende økning av leverenzymer, anamnese med leversykdom, familiær anamnese med arvelig leversykdom, diabetes mellitus, fedme og tidligere eksponering for hepatotoksiske legemidler eller kjemikalier og langvarig metotreksatbehandling. Andre hepatotoksiske legemidler skal ikke gis under metotreksatbehandling med mindre det er helt nødvendig. Inntak av alkohol bør unngås. Nærmere overvåkning av leverenzymer bør utføres ved samtidig bruk av andre hepatotoksiske legemidler. Økt forsiktighet bør utvises ved insulinavhengig diabetes mellitus, da isolerte tilfeller av levercirrhose har oppstått under metotreksatbehandling uten økte transaminaser. |
4. |
Nyrefunksjonen skal overvåkes vha. nyrefunksjonstester og urinanalyse. Hos pasienter med økt sannsynlighet for nedsatt nyrefunksjon (f.eks. hos eldre), bør kontroller utføres oftere. Dette gjelder særlig ved samtidig behandling med legemidler som påvirker eliminasjonen av metotreksat, kan gi nyreskade (f.eks. NSAID) eller som kan føre til redusert blodcelledannelse. Dehydrering kan også intensivere toksisiteten av metotreksat. |
5. |
Vær oppmerksom på symptomer på nedsatt lungefunksjon og om nødvendig må lungefunksjonstest utføres. Påvirkning av lungene krever rask diagnostisering og seponering. Lungesymptomer (særlig tørr, ikke-produktiv hoste) eller ikke-spesifikk pneumonitt som oppstår under behandling, kan være tegn på en potensielt farlig lesjon og kan kreve at behandlingen avbrytes og tilstanden undersøkes nøye. Akutt eller kronisk interstitiell pneumonitt, ofte forbundet med eosinofili i blodet, kan oppstå, og dødsfall er rapportert. Selv om det er kliniske variasjoner, må infeksjoner utelukkes hos typiske pasienter med metotreksatindusert lungesykdom som omfatter feber, hoste, dyspné, hypoksemi og infiltrat på røntgen thorax. Lungesykdommer indusert av metotreksat var ikke alltid fullstendig reversible. Denne lesjonen kan oppstå ved alle doser. Pulmonal alveolær blødning er rapportert ved revmatologiske og relaterte indikasjoner, kan være relatert til vaskulitt og annen komorbiditet. Ved mistanke om dette bør umiddelbare undersøkelser vurderes. |
6. |
Metotreksat kan svekke responsen på vaksinering og påvirke resultatet av immunologiske tester. Spesiell forsiktighet bør utvises ved tilstedeværelse av inaktive, kroniske infeksjoner (f.eks. herpes zoster, tuberkulose, hepatitt B eller C) pga. mulig aktivering. Samtidig vaksinering med levende vaksiner må ikke utføres. |
Interaksjoner
Graviditet, amming og fertilitet
Bivirkninger
Overdosering/Forgiftning
Egenskaper og miljø
Pakninger, priser og refusjon
Metex, INJEKSJONSVÆSKE, oppløsning i ferdigfylt penn:
| Styrke | Pakning Varenr. |
Refusjon | Pris (kr) | R.gr. |
|---|---|---|---|---|
| 7,5 mg | 0,15 ml (ferdigfylt penn, YpsoMate (50 mg/ml)) 147940 |
190,40 (trinnpris 155,40) | C | |
| 6 × 0,15 ml (ferdigfylt penn, YpsoMate (50 mg/ml)) 509024 |
961,50 (trinnpris 751,20) | C | ||
| 10 mg | 0,2 ml (ferdigfylt penn, YpsoMate (50 mg/ml)) 045257 |
218,80 (trinnpris 168,10) | C | |
| 6 × 0,2 ml (ferdigfylt penn, YpsoMate (50 mg/ml)) 059738 |
1 102,00 (trinnpris 827,10) | C | ||
| 12,5 mg | 0,25 ml (ferdigfylt penn, YpsoMate (50 mg/ml)) 548998 |
230,30 (trinnpris 180,40) | C | |
| 6 × 0,25 ml (ferdigfylt penn, YpsoMate (50 mg/ml)) 514102 |
1 179,40 (trinnpris 901,40) | C | ||
| 15 mg | 0,3 ml (ferdigfylt penn, YpsoMate (50 mg/ml)) 197754 |
240,20 (trinnpris 186,10) | C | |
| 6 × 0,3 ml (ferdigfylt penn, YpsoMate (50 mg/ml)) 120248 |
1 256,30 (trinnpris 935,40) | C | ||
| 17,5 mg | 0,35 ml (ferdigfylt penn, YpsoMate (50 mg/ml)) 198195 |
258,40 (trinnpris 199,10) | C | |
| 6 × 0,35 ml (ferdigfylt penn, YpsoMate (50 mg/ml)) 500154 |
1 346,80 (trinnpris 1 013,10) | C | ||
| 20 mg | 0,4 ml (ferdigfylt penn, YpsoMate (50 mg/ml)) 563352 |
269,80 (trinnpris 211,00) | C | |
| 6 × 0,4 ml (ferdigfylt penn, YpsoMate (50 mg/ml)) 541186 |
1 431,90 (trinnpris 1 084,90) | C | ||
| 22,5 mg | 0,45 ml (ferdigfylt penn, YpsoMate (50 mg/ml)) 048113 |
279,10 (trinnpris 225,60) | C | |
| 6 × 0,45 ml (ferdigfylt penn, YpsoMate (50 mg/ml)) 552771 |
1 493,30 (trinnpris 1 172,60) | C | ||
| 25 mg | 0,5 ml (ferdigfylt penn, YpsoMate (50 mg/ml)) 122380 |
279,10 (trinnpris 225,60) | C | |
| 6 × 0,5 ml (ferdigfylt penn, YpsoMate (50 mg/ml)) 496458 |
1 493,30 (trinnpris 1 172,60) | C | ||
| 30 mg | 0,6 ml (ferdigfylt penn, YpsoMate (50 mg/ml)) 128765 |
340,20 | C |
Metex, INJEKSJONSVÆSKE, oppløsning i ferdigfylt sprøyte:
| Styrke | Pakning Varenr. |
Refusjon | Pris (kr) | R.gr. |
|---|---|---|---|---|
| 7,5 mg | 0,15 ml (ferdigfylt glassprøyte u/sikkerhetsmekanisme (50 mg/ml)) 168563 |
190,40 | C | |
| 6 × 0,15 ml (ferdigfylt glassprøyte u/sikkerhetsmekanisme (50 mg/ml)) 370709 |
961,50 | C | ||
| 10 mg | 0,2 ml (ferdigfylt glassprøyte u/sikkerhetsmekanisme (50 mg/ml)) 168574 |
218,80 | C | |
| 6 × 0,2 ml (ferdigfylt glassprøyte u/sikkerhetsmekanisme (50 mg/ml)) 444728 |
1 102,00 | C | ||
| 12,5 mg | 0,25 ml (ferdigfylt glassprøyte u/sikkerhetsmekanisme (50 mg/ml)) 569888 |
230,30 | C | |
| 15 mg | 0,3 ml (ferdigfylt glassprøyte u/sikkerhetsmekanisme (50 mg/ml)) 168585 |
240,20 | C | |
| 6 × 0,3 ml (ferdigfylt glassprøyte u/sikkerhetsmekanisme (50 mg/ml)) 174679 |
1 256,30 | C | ||
| 17,5 mg | 0,35 ml (ferdigfylt glassprøyte u/sikkerhetsmekanisme (50 mg/ml)) 451093 |
258,40 | C | |
| 20 mg | 0,4 ml (ferdigfylt glassprøyte u/sikkerhetsmekanisme (50 mg/ml)) 168596 |
269,80 | C | |
| 6 × 0,4 ml (ferdigfylt glassprøyte u/sikkerhetsmekanisme (50 mg/ml)) 144452 |
1 431,90 | C | ||
| 22,5 mg | 0,45 ml (ferdigfylt glassprøyte u/sikkerhetsmekanisme (50 mg/ml)) 422475 |
279,10 | C | |
| 25 mg | 0,5 ml (ferdigfylt glassprøyte u/sikkerhetsmekanisme (50 mg/ml)) 168607 |
279,10 | C | |
| 6 × 0,5 ml (ferdigfylt glassprøyte u/sikkerhetsmekanisme (50 mg/ml)) 552464 |
1 493,30 | C | ||
| 30 mg | 0,6 ml (ferdigfylt glassprøyte u/sikkerhetsmekanisme (50 mg/ml)) 566253 |
340,20 | C |
Metotreksat
Legemidler: Ebetrex konsentrat til infusjonsvæske, Metex injeksjonsvæske, Methofill injeksjonsvæske, Methotrexat injeksjonsvæske, Methotrexat konsentrat til infusjonsvæske, Nordimet injeksjonsvæske
Indikasjon: Crohns sykdom hos barn og ungdom (til og med 17 år). Ulcerøs kolitt hos barn og ungdom (til og med 17 år). Uveitt (iridosyklitt, chorioretinal betennelse) - hos barn og ungdom (til og med 17 år). Tilleggsbehandling – ved behandling med adalimumab eller infliksimab. Atopisk eksem/dermatitt - hos barn og ungdom (til og med 17 år).
For blåreseptsøknad og -vedtak, se Tjenesteportal for helseaktører
SPC (preparatomtale)
Metex INJEKSJONSVÆSKE, oppløsning i ferdigfylt penn 7,5 mg |
Metex INJEKSJONSVÆSKE, oppløsning i ferdigfylt penn 10 mg |
Metex INJEKSJONSVÆSKE, oppløsning i ferdigfylt penn 12,5 mg |
Metex INJEKSJONSVÆSKE, oppløsning i ferdigfylt penn 15 mg |
Metex INJEKSJONSVÆSKE, oppløsning i ferdigfylt penn 17,5 mg |
Metex INJEKSJONSVÆSKE, oppløsning i ferdigfylt penn 20 mg |
Metex INJEKSJONSVÆSKE, oppløsning i ferdigfylt penn 22,5 mg |
Metex INJEKSJONSVÆSKE, oppløsning i ferdigfylt penn 25 mg |
Metex INJEKSJONSVÆSKE, oppløsning i ferdigfylt penn 30 mg |
Metex INJEKSJONSVÆSKE, oppløsning i ferdigfylt sprøyte 7,5 mg Metex INJEKSJONSVÆSKE, oppløsning i ferdigfylt sprøyte 10 mg Metex INJEKSJONSVÆSKE, oppløsning i ferdigfylt sprøyte 12,5 mg Metex INJEKSJONSVÆSKE, oppløsning i ferdigfylt sprøyte 15 mg Metex INJEKSJONSVÆSKE, oppløsning i ferdigfylt sprøyte 17,5 mg Metex INJEKSJONSVÆSKE, oppløsning i ferdigfylt sprøyte 20 mg Metex INJEKSJONSVÆSKE, oppløsning i ferdigfylt sprøyte 22,5 mg Metex INJEKSJONSVÆSKE, oppløsning i ferdigfylt sprøyte 25 mg Metex INJEKSJONSVÆSKE, oppløsning i ferdigfylt sprøyte 30 mg |
Penn: 18.09.2024
Sprøyte: 06.10.2025
Sist endret: 26.09.2024
(priser og ev. refusjon oppdateres hver 14. dag)