Dette er et søkefelt med autofullføringsforslag. Start å skrive og du vil få opp forslag på virkestoff, legemidler og bruksområder, som du kan velge mellom. Bruk Søke-knappen hvis autofullføringsforslagene ikke er relevante, eller Strekkode-knappen hvis du ønsker å skanne strekkoden på legemiddelpakningen.
Virkestoff: Koagulasjonsfaktor VIII, Simoktokog alfa
Pakningsvedlegg
Pakningsvedlegg: Informasjon til brukeren
Nuwiq 250 IE pulver og væske til injeksjonsvæske, oppløsning
Nuwiq 500 IE pulver og væske til injeksjonsvæske, oppløsning
Nuwiq 1000 IE pulver og væske til injeksjonsvæske, oppløsning
Nuwiq 1500 IE pulver og væske til injeksjonsvæske, oppløsning
Nuwiq 2000 IE pulver og væske til injeksjonsvæske, oppløsning
Nuwiq 2500 IE pulver og væske til injeksjonsvæske, oppløsning
Nuwiq 3000 IE pulver og væske til injeksjonsvæske, oppløsning
Nuwiq 4000 IE pulver og væske til injeksjonsvæske, oppløsning
simoctocog alfa (rekombinant human koagulasjonsfaktor VIII)
Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder informasjon som er viktig for deg.
-
Ta vare på dette pakningsvedlegget. Du kan få behov for å lese det igjen.
-
Spør lege hvis du har flere spørsmål eller trenger mer informasjon.
-
Dette legemidlet er skrevet ut kun til deg. Ikke gi det videre til andre. Det kan skade dem, selv om de har symptomer på sykdom som ligner dine.
-
Kontakt lege dersom du opplever bivirkninger, inkludert mulige bivirkninger som ikke er nevnt i dette pakningsvedlegget. Se avsnitt 4.
-
I dette pakningsvedlegget finner du informasjon om:
- Hva Nuwiq er og hva det brukes mot
- Hva du må vite før du bruker Nuwiq
- Hvordan du bruker Nuwiq
- Mulige bivirkninger
- Hvordan du oppbevarer Nuwiq
- Innholdet i pakningen og ytterligere informasjon
1. Hva Nuwiq er og hva det brukes mot
Nuwiq inneholder virkestoffet human rekombinant koagulasjonsfaktor VIII (simoctocog alfa). Faktor VIII er nødvendig for at blodet skal levre seg (koagulere) og stanse blødning. Pasienter med hemofili A (medfødt mangel på faktor VIII) mangler faktor VIII eller den fungerer ikke slik den skal.
Nuwiq erstatter manglende faktor VIII og brukes for å behandle og forebygge blødning hos pasienter med hemofili A. Nuwiq kan brukes i alle aldersgrupper.
Nuwiq erstatter manglende faktor VIII og brukes for å behandle og forebygge blødning hos pasienter med hemofili A. Nuwiq kan brukes i alle aldersgrupper.
2. Hva du må vite før du bruker Nuwiq
Bruk ikke Nuwiq
-
dersom du er allergisk overfor virkestoffet simoctocog alfa eller noen av de andre innholdsstoffene i dette legemidlet (listet opp i avsnitt 6).
Advarsler og forsiktighetsregler
Snakk med lege før du bruker Nuwiq.
Det er en liten risiko for at du kan få en anafylaktisk reaksjon (kraftig, plutselig allergisk reaksjon) mot Nuwiq. Du bør kjenne til de tidlige tegnene på allergiske reaksjoner som er angitt i avsnitt 4 "Allergiske reaksjoner".
Hvis noen av disse symptomene oppstår, så stopp injeksjonen umiddelbart og ta kontakt med legen din.
Hvis noen av disse symptomene oppstår, så stopp injeksjonen umiddelbart og ta kontakt med legen din.
Utvikling av inhibitorer (antistoffer) er en kjent komplikasjon som kan oppstå ved behandling med alle faktor VIII-legemidler. Disse inhibitorene, spesielt ved høye nivåer, hindrer at behandlingen virker som den skal, og du eller barnet ditt vil overvåkes nøye for utvikling av disse inhibitorene. Kontakt legen din umiddelbart dersom blødningen din eller til barnet ditt ikke kan kontrolleres med Nuwiq.
Kardiovaskulære hendelser
Hos pasienter med eksisterende kardiovaskulære risikofaktorer kan substitusjonsbehandling med faktor VIII øke kardiovaskulær risiko.
Hos pasienter med eksisterende kardiovaskulære risikofaktorer kan substitusjonsbehandling med faktor VIII øke kardiovaskulær risiko.
Kateterrelaterte komplikasjoner
Hvis utstyr for sentral venetilgang (CVAD) er nødvendig, må risikoen for CVAD-relaterte komplikasjoner, inkludert lokale infeksjoner, bakteriemi og trombose på kateterstedet vurderes.
Hvis utstyr for sentral venetilgang (CVAD) er nødvendig, må risikoen for CVAD-relaterte komplikasjoner, inkludert lokale infeksjoner, bakteriemi og trombose på kateterstedet vurderes.
Det er viktig å notere batchnummeret for din pakning med Nuwiq.
Hver gang du får en ny pakning med Nuwiq, må du notere dato og batchnummer (som er angitt på pakningen etter Lot) og oppbevare denne informasjonen på et sikkert sted.
Hver gang du får en ny pakning med Nuwiq, må du notere dato og batchnummer (som er angitt på pakningen etter Lot) og oppbevare denne informasjonen på et sikkert sted.
Andre legemidler og Nuwiq
Snakk med lege dersom du bruker, nylig har brukt eller planlegger å bruke andre legemidler.
Graviditet og amming
Snakk med lege eller apotek før du tar dette legemidlet dersom du er gravid eller ammer, tror at du kan være gravid eller planlegger å bli gravid.
Kjøring og bruk av maskiner
Nuwiq påvirker ikke evnen til å kjøre bil og bruke maskiner.
Nuwiq inneholder natrium
Dette legemidlet inneholder 18,4 mg natrium (finnes i bordsalt) i hvert hetteglass. Dette tilsvarer 0,92 % av den anbefalte maksimale daglige dosen av natrium gjennom dietten for en voksen person.
3. Hvordan du bruker Nuwiq
Behandling med Nuwiq vil startes av en lege med erfaring i behandling av pasienter med hemofili A. Bruk alltid dette legemidlet nøyaktig slik legen eller sykepleieren har angitt. Kontakt lege eller sykepleier hvis du er usikker.
Nuwiq injiseres vanligvis inn i en vene (intravenøst) av en lege eller sykepleier med erfaring i behandling av pasienter med hemofili A. Bare etter tilstrekkelig opplæring kan du eller andre personer gi en Nuwiq-injeksjon.
Legen beregner dosen du skal ha med Nuwiq (i internasjonale enheter = IE) ut fra din tilstand og kroppsvekt, og ut fra om legemidlet skal brukes til forebygging eller behandling av blødning. Hvor ofte du trenger en injeksjon, avhenger av hvor godt legemidlet virker på deg. Vanligvis varer behandling for hemofili A livet ut.
Forebygging av blødning
Vanlig dose Nuwiq er fra 20 til 40 IE per kg kroppsvekt, gitt hver 2. til 3. dag. I noen tilfeller, og spesielt hos yngre pasienter, kan det imidlertid være nødvendig med hyppigere injeksjoner eller høyere doser.
Vanlig dose Nuwiq er fra 20 til 40 IE per kg kroppsvekt, gitt hver 2. til 3. dag. I noen tilfeller, og spesielt hos yngre pasienter, kan det imidlertid være nødvendig med hyppigere injeksjoner eller høyere doser.
Behandling av blødning
Dosen med Nuwiq beregnes ut fra kroppsvekt og faktor VIII-nivåene som skal oppnås. Ønsket nivå for faktor VIII avhenger av hvor alvorlig blødningen er og hvor du blør.
Dosen med Nuwiq beregnes ut fra kroppsvekt og faktor VIII-nivåene som skal oppnås. Ønsket nivå for faktor VIII avhenger av hvor alvorlig blødningen er og hvor du blør.
Snakk med legen dersom du tror at Nuwiq ikke har god nok effekt. Legen vil utføre relevante laboratorietester for å sikre at du har tilstrekkelig høye nivåer faktor VIII. Dette er spesielt viktig hvis du skal gjennomgå en større operasjon.
Pasienter som utvikler faktor VIII-inhibitorer
Hvis du ikke oppnår forventede nivåer av faktor VIII i blodet med Nuwiq, eller hvis blødninger ikke lar seg kontrollere godt nok, kan det skyldes utvikling av faktor VIII-inhibitorer. Legen vil undersøke dette. Det kan hende at du trenger høyere doser av Nuwiq eller et annet preparat for å kontrollere blødninger. Ikke øk den totale dosen av Nuwiq for å kontrollere blødninger uten å ha snakket med legen din.
Bruk hos barn og ungdom
Hvis du ikke oppnår forventede nivåer av faktor VIII i blodet med Nuwiq, eller hvis blødninger ikke lar seg kontrollere godt nok, kan det skyldes utvikling av faktor VIII-inhibitorer. Legen vil undersøke dette. Det kan hende at du trenger høyere doser av Nuwiq eller et annet preparat for å kontrollere blødninger. Ikke øk den totale dosen av Nuwiq for å kontrollere blødninger uten å ha snakket med legen din.
Bruksmåten for Nuwiq hos barn og ungdom skiller seg ikke fra bruksmåten hos voksne. Fordi det kan være nødvendig å gi faktor VIII oftere til barn og ungdom, kan det bli nødvendig å bruke utstyr for sentral venetilgang (CVAD). En CVAD er en ekstern kobling som gir tilgang til blodstrømmen gjennom et kateter uten injeksjon gjennom huden.
Dersom du tar for mye av Nuwiq
Ingen symptomer på overdosering har vært rapportert. Kontakt legen din dersom du har injisert mer Nuwiq enn du bør.
Dersom du har glemt å ta Nuwiq
Du skal ikke ta dobbel dose som erstatning for en glemt dose. Ta neste dose umiddelbart og fortsett som anbefalt av lege.
Dersom du avbryter behandling med Nuwiq
Ikke slutt å bruke Nuwiq uten å snakke med lege.
Spør lege dersom du har noen spørsmål om bruken av dette legemidlet.
4. Mulige bivirkninger
Vanlige bivirkninger forekommer hos inntil 1 av 10 personer
Som alle legemidler kan dette legemidlet forårsake bivirkninger, men ikke alle får det.
Stopp bruken av dette legemidlet umiddelbart og oppsøk umiddelbart medisinsk hjelp dersom:
-
du merker symptomer på allergiske reaksjoner
Allergiske reaksjoner kan inkludere utslett, elveblest, urtikaria (kløende utslett), herunder generalisert urtikaria, opphovning av lepper og tunge, kortpustethet, pipende pust, sammensnøring i brystet, oppkast, rastløshet, lavt blodtrykk og svimmelhet. Disse symptomene kan være tidlige symptomer på anafylaktisk sjokk. Dersom det oppstår alvorlige, plutselige allergiske reaksjoner (anafylaksi) (svært sjeldne: forekommer hos inntil 1 av 10 000 personer), må injeksjonen stoppes umiddelbart, og du må med én gang kontakte lege.
Alvorlige symptomer krever øyeblikkelig behandling. -
du legger merke til at legemidlet slutter å virke som det skal (blødning stoppes ikke, eller de oppstår hyppigere)
Hos barn og ungdom som ikke tidligere har vært behandlet med faktor VIII-legemidler, er utvikling av inhibitorantistoffer (se avsnitt 2) svært vanlig (flere enn 1 av 10 pasienter).
Hos pasienter som tidligere har fått behandling med faktor VIII (behandling i mer enn 150 dager), er imidlertid risikoen mindre vanlig (færre enn 1 av 100 pasienter). Dersom dette skjer, kan legemidlet du eller barnet ditt bruker slutte å virke som det skal, og du eller barnet ditt kan oppleve at blødningen vedvarer. Kontakt legen din umiddelbart dersom dette skjer.
Overfølsomhet, feber.
Mindre vanlige bivirkninger forekommer hos inntil 1 av 100 personer
Prikking eller nummenhet (parestesi), hodepine, svimmelhet, vertigo, åndenød, munntørrhet, ryggsmerter, betennelse på injeksjonsstedet, smerter på injeksjonsstedet, generell sykdomsfølelse (uvelhet), hemoragisk anemi, anemi, brystsmerter, positiv for ikke-nøytraliserende antistoff (hos tidligere behandlede pasienter).
Melding av bivirkninger
Kontakt lege, apotek eller sykepleier dersom du opplever bivirkninger. Dette gjelder også bivirkninger som ikke er nevnt i pakningsvedlegget. Du kan også melde fra om bivirkninger direkte via meldeskjema som finnes på nettsiden til Direktoratet for medisinske produkter: www.dmp.no/pasientmelding. Ved å melde fra om bivirkninger bidrar du med informasjon om sikkerheten ved bruk av dette legemidlet.
5. Hvordan du oppbevarer Nuwiq
Oppbevares utilgjengelig for barn.
Bruk ikke dette legemidlet etter utløpsdatoen som er angitt på esken og hetteglassets etikett etter "EXP". Utløpsdatoen er den siste dagen i den angitte måneden.
Oppbevares i kjøleskap (2-8ºC). Skal ikke fryses. Oppbevar hetteglasset i originalpakningen for å beskytte mot lys.
Før rekonstituering kan Nuwiq-pulveret oppbevares ved romtemperatur (høyst 25ºC) i én enkelt periode på maksimalt 1 måned. Startdatoen for oppbevaring av Nuwiq ved romtemperatur skal noteres på esken. Nuwiq skal ikke oppbevares i kjøleskap igjen etter å ha vært oppbevart ved romtemperatur. Bruk rekonstituert oppløsning umiddelbart etter rekonstituering.
Bruk ikke dette legemidlet hvis du oppdager synlige tegn på forringelse på pakningens forsegling, særlig på sprøyten og/eller hetteglasset.
Legemidler skal ikke kastes i avløpsvann eller sammen med husholdningsavfall. Spør på apoteket hvordan du skal kaste legemidler som du ikke lenger bruker. Disse tiltakene bidrar til å beskytte miljøet.
6. Innholdet i pakningen og ytterligere informasjon
Sammensetning av Nuwiq
Pulver:
-
Virkestoffet er rekombinant human koagulasjonsfaktor VIII (simoctocog alfa).
Hvert hetteglass med pulver inneholder 250, 500, 1000, 1500, 2000, 2500, 3000 eller 4000 IE simoctocog alfa.
Hver rekonstituerte oppløsning inneholder ca. 100, 200, 400, 600, 800, 1000, 1200 eller 1600 IE/ml simoctocog alfa. -
Andre innholdsstoffer er sukrose, natriumklorid, kalsiumkloriddihydrat, argininhydroklorid, natriumsitratdihydrat og poloksamer 188. Se avsnitt 2, "Nuwiq inneholder natrium".
Oppløsningsvæske:
Vann til injeksjonsvæsker
Vann til injeksjonsvæsker
Hvordan Nuwiq ser ut og innholdet i pakningen
Nuwiq leveres som pulver og væske til injeksjonsvæske, oppløsning. Pulveret er et hvitt til off-white pulver i et hetteglass. Oppløsningsvæsken er vann til injeksjonsvæsker i en ferdigfylt glassprøyte.
Etter rekonstituering er oppløsningen klar, fargeløs og uten partikler. Hver pakning med Nuwiq inneholder:
Etter rekonstituering er oppløsningen klar, fargeløs og uten partikler. Hver pakning med Nuwiq inneholder:
-
1 hetteglass med pulver 250, 500, 1000, 1500, 2000, 2500, 3000 eller 4000 IE simoctocog alfa
-
1 ferdigfylt sprøyte med 2,5 ml vann til injeksjonsvæsker
-
1 hetteglassadapter
-
1 venekanyle
-
2 desinfeksjonsservietter
Innehaver av markedsføringstillatelsen og tilvirker
Octapharma AB, Lars Forssells gata 23, 112 75 Stockholm, Sverige
Ta kontakt med den lokale representanten for innehaveren av markedsføringstillatelsen for ytterligere informasjon om dette legemidlet:
Ta kontakt med den lokale representanten for innehaveren av markedsføringstillatelsen for ytterligere informasjon om dette legemidlet:
Octapharma AS
Tlf: +47 63988860
Tlf: +47 63988860
Dette pakningsvedlegget ble sist oppdatert 23.10.2025
Detaljert informasjon om dette legemidlet er tilgjengelig på nettstedet til Det Europeiske legemiddelkontoret (the European Medicines Agency): https://www.ema.europa.eu
Behandling etter behov
Mengden som skal administreres og administreringshyppigheten skal alltid tilpasses klinisk effekt i hvert enkelt tilfelle.
Ved følgende blødningstilstander skal faktor VIII-aktiviteten ikke falle under det angitte aktivitetsnivået i plasma (i % av normalen eller IE/dl) i den relevante perioden. Følgende tabell kan brukes som veiledning for dosering ved blødningsepisoder og kirurgi.
INSTRUKSJONER FOR TILBEREDNING OG ADMINISTRERING
Mengden som skal administreres og administreringshyppigheten skal alltid tilpasses klinisk effekt i hvert enkelt tilfelle.
Ved følgende blødningstilstander skal faktor VIII-aktiviteten ikke falle under det angitte aktivitetsnivået i plasma (i % av normalen eller IE/dl) i den relevante perioden. Følgende tabell kan brukes som veiledning for dosering ved blødningsepisoder og kirurgi.
1. La sprøyten med oppløsningsvæske (vann til injeksjonsvæsker) og pulveret i det uåpnede hetteglasset nå romtemperatur. Du kan gjøre dette ved å holde dem i hendene til de føles like varme som hendene. Varm ikke opp hetteglasset og den ferdigfylte sprøyten på noen annen måte. Denne temperaturen skal opprettholdes under rekonstituering.
2. Fjern "flip-off"-hetten i plast fra hetteglasset med pulver slik at midten av gummiproppen er synlig. Ikke fjern den gråfargede proppen eller metallringen rundt toppen av hetteglasset.

3. Tørk toppen av hetteglasset med en desinfeksjonsserviett. La alkoholen tørke.
2. Fjern "flip-off"-hetten i plast fra hetteglasset med pulver slik at midten av gummiproppen er synlig. Ikke fjern den gråfargede proppen eller metallringen rundt toppen av hetteglasset.

3. Tørk toppen av hetteglasset med en desinfeksjonsserviett. La alkoholen tørke.
4. Trekk beskyttelsespapiret av pakningen med hetteglassadapteren. Ikke ta adapteren ut av emballasjen.


5. Sett hetteglasset med pulver på en jevn overflate og hold det fast. Ta tak i pakningen med adapteren og plasser hetteglassadapteren over midten av gummiproppen på hetteglasset med pulver. Trykk adapterpakningen bestemt ned til adapterspissen trenger igjennom gummiproppen. Adapteren vil da klikke på plass på hetteglasset.


6. Trekk beskyttelsespapiret av pakningen med den ferdigfylte sprøyten. Hold i enden av stempelet, og unngå berøring med selve staven. Fest den gjengede enden av stempelet til stempeldelen i sprøyten med oppløsningsvæske. Drei sprøytestempelet med urviseren til du kjenner lett motstand.


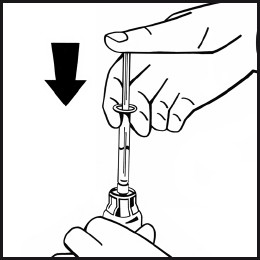
7. Brekk av forseglingsspissen av plast på sprøyten med oppløsningsvæske ved å brekke langs perforeringen på hetten. Ikke berør innsiden av hetten eller tuppen på sprøyten. Hvis oppløsningen ikke brukes umiddelbart, skal den ferdigfylte sprøyten lukkes med forseglingsspissen for oppbevaring.
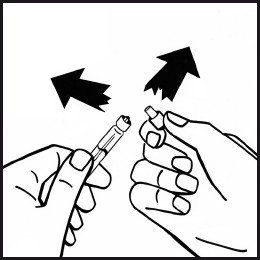
8. Ta av adapterens emballasje og kast den.

8. Ta av adapterens emballasje og kast den.
9. Koble sprøyten med oppløsningsvæske til hetteglassadapteren ved å dreie med urviseren til du kjenner motstand.


10. Injiser all oppløsningsvæske langsomt inn i hetteglasset med pulver ved å trykke ned sprøytestempelet.
11. Løs opp pulveret ved å forsiktig bevege eller svinge på hetteglasset noen ganger i sirkulære bevegelser uten å ta ut sprøyten. Må ikke rystes. Vent til alt pulveret er helt oppløst.
12. Inspiser den ferdige oppløsningen med hensyn til partikler før administrering. Oppløsningen skal være klar og fargeløs, og uten synlige partikler. Ikke bruk oppløsninger som er uklare eller har bunnfall.
13. Vend hetteglasset med sprøyten opp-ned, og trekk den ferdige oppløsningen langsomt inn i sprøyten. Sørg for at alt innholdet i hetteglasset overføres til sprøyten.

12. Inspiser den ferdige oppløsningen med hensyn til partikler før administrering. Oppløsningen skal være klar og fargeløs, og uten synlige partikler. Ikke bruk oppløsninger som er uklare eller har bunnfall.
13. Vend hetteglasset med sprøyten opp-ned, og trekk den ferdige oppløsningen langsomt inn i sprøyten. Sørg for at alt innholdet i hetteglasset overføres til sprøyten.

14. Koble den fylte sprøyten fra hetteglassadapteren ved å dreie mot urviseren. Kast det tomme hetteglasset.
15. Oppløsningen er nå klar til bruk umiddelbart. Skal ikke oppbevares i kjøleskap.
16. Rengjør det valgte injeksjonsstedet med en av de medfølgende desinfeksjonsserviettene.
17. Fest medfølgende infusjonssett til sprøyten.
Sett kanylen på infusjonssettet inn i den valgte venen. Har du brukt et stasebånd for å gjøre venen mer synlig, slipper du opp stasebåndet før du begynner å injisere oppløsningen.
Det må ikke komme blod inn i sprøyten på grunn av risiko for dannelse av fibrinklumper.
Sett kanylen på infusjonssettet inn i den valgte venen. Har du brukt et stasebånd for å gjøre venen mer synlig, slipper du opp stasebåndet før du begynner å injisere oppløsningen.
Det må ikke komme blod inn i sprøyten på grunn av risiko for dannelse av fibrinklumper.
18. Injiser oppløsningen langsomt inn i venen, ikke raskere enn 4 ml per minutt.
Hvis du bruker mer enn ett hetteglass med pulver til én behandling, kan samme injeksjonskanyle brukes om igjen. Hetteglassadapteren og sprøyten er kun til engangsbruk.