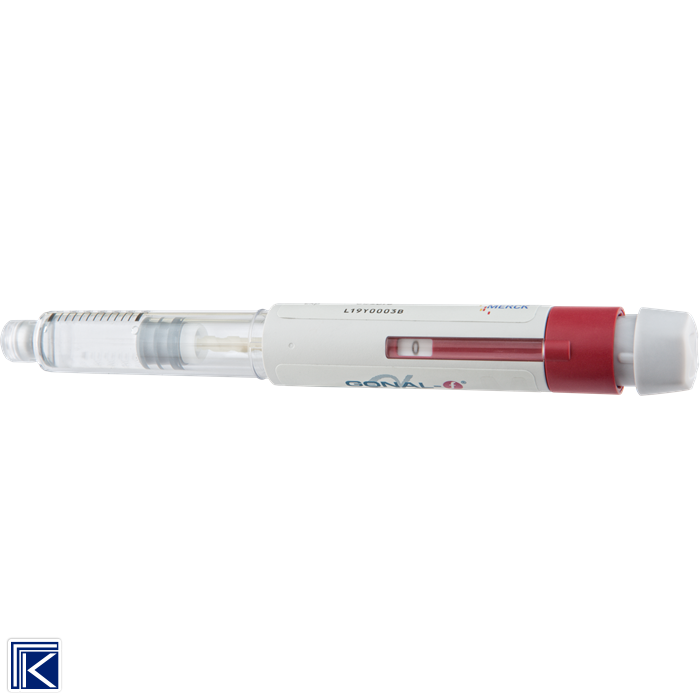
INJEKSJONSVÆSKE, oppløsning i ferdigfylt penn 300 IE/0,48 ml: Hver ferdigfylt penn inneh.: Follitropin alfa (r-hFSH) 300 IE, Poloksamer 188, sukrose, metionin, natriumdihydrogenfosfatmonohydrat, dinatriumfosfatdihydrat, m-kresol, konsentrert fosforsyre, natriumhydroksid, vann til injeksjonsvæsker.
INJEKSJONSVÆSKE, oppløsning i ferdigfylt penn 450 IE/0,72 ml: Hver ferdigfylt penn inneh.: Follitropin alfa (r-hFSH) 450 IE, Poloksamer 188, sukrose, metionin, natriumdihydrogenfosfatmonohydrat, dinatriumfosfatdihydrat, m-kresol, konsentrert fosforsyre, natriumhydroksid, vann til injeksjonsvæsker.
INJEKSJONSVÆSKE, oppløsning i ferdigfylt penn 900 IE/1,44 ml: Hver ferdigfylt penn inneh.: Follitropin alfa (r-hFSH) 900 IE, Poloksamer 188, sukrose, metionin, natriumdihydrogenfosfatmonohydrat, dinatriumfosfatdihydrat, m-kresol, konsentrert fosforsyre, natriumhydroksid, vann til injeksjonsvæsker.
Indikasjoner
Voksne kvinner:- Anovulasjon (inkl. polycystisk ovariesyndrom, PCOS) hos kvinner som ikke har respondert på behandling med klomifensitrat.
- Stimulering av multippel follikkelutvikling hos kvinner som gjennomgår superovulasjon i forbindelse med assisterte fertilitetsteknikker som f.eks. in vitro-fertilisering (IVF), gamet-intra-fallopisk transfer eller zygot-intrafallopisk transfer.
- Follitropin alfa i kombinasjon med et luteiniserende hormon (LH) er indisert for stimulering av follikulær utvikling hos kvinner med alvorlig LH- og FSH-mangel.
- Follitropin alfa kan gis sammen med humant koriongonadotropin (hCG) ved stimulering av spermatogenese hos menn som har medfødt eller ervervet hypogonadisme.
Dosering
Mht. sporbarhet skal preparatnavn og batchnr. noteres i pasientjournalen. Behandling med follitropin alfa bør utføres av spesialist med erfaring i behandling av fertilitetsproblemer. Daglig dosering, behandlingsregimer og overvåkning bør være individuelt tilpasset for å optimalisere follikulær utvikling og for å redusere risikoen for uønsket ovarial hyperstimulering. Det anbefales at doseringen nedenfor følges. Tilsvarende doser av monodose- og multidose-formuleringen av GONAL-f er bioekvivalente.- Nedsatt lever-/nyrefunksjon: Sikkerhet, effekt og farmakokinetikk er ikke fastslått.
- Barn og ungdom: Bruk er ikke relevant.
- Eldre: Bruk er ikke relevant. Sikkerhet og effekt er ikke fastslått.
Kontraindikasjoner
Overfølsomhet for innholdsstoffene. Tumor i hypothalamus eller hypofysen. Kvinner: Ovarieforstørrelse eller cyste som ikke er relatert til PCOS og er av ukjent opprinnelse. Gynekologisk blødning av ukjent årsak. Ovarial-, livmor- eller brystkreft. Når effektiv respons ikke kan oppnås, som ved: Kvinner: Primær ovarialsvikt. Misdannelser i kjønnsorganene som er uforenlig med graviditet. Fibromyomer i uterus som er uforenlig med graviditet. Menn: Primær testikulær insuffisiens.Forsiktighetsregler
Generelle anbefalinger: Potent gonadotropt middel som kan forårsake milde til alvorlige bivirkninger. Må bare brukes av leger med lang erfaring i behandling av fertilitetsproblemer. Gonadotropinbehandling krever en viss tidsforpliktelse av lege/annet helsepersonell, samt tilgjengelighet av aktuelt monitoreringsutstyr. Regelmessig kontroll av ovarialrespons med ultralyd, enten alene eller med samtidig måling av serumøstradiolnivåer, er påkrevd for effektiv bruk. Det kan være en viss forskjell i behandlingsrespons på FSH mellom pasienter, med dårlig respons hos noen. Lavest effektiv dose bør benyttes hos både menn og kvinner. Porfyri: Pasienter med porfyri eller med porfyri i familien, skal kontrolleres nøye under behandling. Dersom porfyri oppstår eller forverres kan seponering være nødvendig. Behandling av kvinner: Før behandlingsoppstart bør parets infertilitet bedømmes og mulige kontraindikasjoner mot graviditet vurderes. Pasienten bør særlig vurderes mht. hypotyreoidisme, adrenokortikal svikt, hyperprolaktinemi og egnet behandling bør gis. Pasienter som gjennomgår stimulering av follikkelvekst, enten ved behandling for infertilitet pga. anovulasjon eller ved assistert befruktning, kan oppleve ovarieforstørrelse eller hyperstimulering. Forekomst av slike tilfeller reduseres ved å følge anbefalt behandling og ved nøye monitorering. Riktig fortolkning av tegn på follikkelutvikling og modning krever oppfølging av spesialist med erfaring i fortolkning av disse prøvene. Økt ovariell sensitivitet er sett i kliniske utprøvinger når follitropin alfa administreres med lutropin alfa. Dersom daglig FSH-dose skal økes, bør dosetilpasning skje med 7-14 dagers intervaller og med doseøkning på 37,5-75 IE. Direkte sammenligning av follitropin alfa/LH mot humant menopausalt gonadotropin (hMG) er ikke utført. Sammenligning av historiske data kan tyde på at ovulasjonsraten som oppnås med follitropin alfa/LH er lik den som oppnås med hMG. Ovarialt hyperstimuleringssyndrom (OHSS): Er en medisinsk komplikasjon som må skilles fra ukomplisert ovarieforstørrelse. OHSS kan manifesteres med økende alvorlighetsgrader, og omfatter uttalt ovarieforstørrelse, høye serumkonsentrasjoner av gonadale steroider og økt vaskulær permeabilitet som kan føre til ansamling av væske i peritonealhulen, pleurahulen og perikard (sjelden). Symptomer ved alvorlige tilfeller av OHSS: Abdominalsmerte, abdominal distensjon, alvorlig ovarieforstørrelse, vektøkning, dyspné, oliguri og gastrointestinale symptomer, bl.a. kvalme, oppkast og diaré. Klinisk undersøkelse kan vise hypovolemi, hemokonsentrasjon, elektrolyttforstyrrelser, ascites, hemoperitoneum, pleuravæske, hydrothorax eller akutt åndenød. Svært sjelden kan alvorlige tilfeller av OHSS forverres av ovarievridning eller tromboemboliske komplikasjoner som lungeemboli, iskemisk slag og myokardinfarkt. Uavhengige risikofaktorer for utvikling av OHSS inkluderer ung alder, slank kropp, polycystisk ovarialsyndrom, høyere doser av eksogene gonadotropiner, høyt absolutt eller raskt stigende serumøstradiolnivå og tidligere episoder med OHSS, et stort antall utviklende follikler og et stort antall oocytter hentet fra sykluser med assistert befruktningsteknologi (ART). Ved bruk av anbefalt follitropin alfadose og administreringsregime kan minimere risikoen for ovarial hyperstimuli. Overvåkning av stimulisykluser ved bruk av ultralyd i tillegg til østradiolmålinger anbefales for tidlig identifisering av risikofaktorer. hCG kan spille en nøkkelrolle ved utløsning av OHSS og at syndromet kan være mer alvorlig og langvarig hvis graviditet forekommer. Forekommer tegn på ovarial hyperstimulering, som f.eks. >5500 pg/ml eller >20 200 pmol/liter og/eller ≥40 follikler totalt, anbefales det at hCG holdes tilbake og pasienten rådes til å avstå fra samleie eller bruke mekaniske prevensjonsmidler i minst 4 dager. OHSS kan utvikles raskt (innen 24 timer til flere dager) til å bli en alvorlig medisinsk tilstand. Oftest opptrer OHSS etter at hormonbehandlingen seponeres og når maksimum etter ca. 7-10 dager. Pasientene bør derfor følges opp i minst 2 uker etter hCG-administrering. Ved assistert befruktning kan aspirasjon av alle follikler før ovulasjon redusere forekomsten av hyperstimulering. Dersom alvorlig OHSS forekommer bør gonadotropinbehandlingen avbrytes, pasienten legges inn i sykehus og egnet behandling påbegynnes. Syndromet forekommer oftere hos pasienter med PCOS og går som regel tilbake uten behandling. Multippel graviditet: Multippel graviditet, særlig med høyt antall, innebærer økt risiko for maternelle og perinatale komplikasjoner. Sammenlignet med naturlig befruktning øker hyppigheten av multippel graviditet og flerlingfødsler hos pasienter som gjennomgår ovulasjonsinduksjon med follitropin alfa. De fleste av disse er tvillinger. For å redusere risikoen for multippel graviditet anbefales nøye kontroll av ovarialrespons. Ved assistert befruktning er risikoen for multippel graviditet relatert til antall embryo som blir tilbakeført, embryoenes kvalitet og pasientens alder. Før behandlingsstart bør pasienter opplyses om risikoen for flerlingfødsel. Spontanabort: Forekomsten av spontanabort er større hos pasienter som gjennomgår stimulering av follikkelutvikling for ovulasjonsinduksjon eller assistert befruktning. Ektopisk graviditet: Kvinner med sykdom i egglederne i anamnesen har risiko for ektopisk graviditet, enten graviditeten skyldes spontan eller assistert befruktning. Forekomst av ektopisk graviditet etter IVF er rapportert som høyere enn ellers i befolkningen. Neoplasmer i reproduksjonssystemet: Ovarialcancer og andre neoplasmer i reproduksjonssystemet er rapportert, både benigne og maligne, hos kvinner som har gjennomgått multiple regimer for infertilitetsbehandling. Det er ikke klarlagt om behandling med gonadotropiner øker risiko for slike tumorer eller ikke hos infertile kvinner. Medfødte misdannelser: Forekomsten av medfødte misdannelser kan være noe høyere etter assistert befruktning enn etter spontane graviditeter. Dette antar man kan komme av forskjeller i parenterale karakteristika (f.eks. maternell alder, sædcellekarakteristika) og flerlingesvangerskap. Tromboembolisme: Hos kvinner med nylig eller pågående tromboembolisk sykdom eller kvinner som har en forhøyet risiko for tromboembolisme, kan behandling med gonadotropiner ytterligere øke risikoen for forverring eller forekomst av slike hendelser. Hos disse kvinnene må fordelene med behandling med gonadotropiner veies opp mot risikoen. Det skal også poengteres at graviditet i seg selv, i tillegg til OHSS, også øker risiko for tromboembolisme. Behandling hos menn: Forhøyede endogene FSH-nivåer er tegn på primær testikulær svikt. Slike pasienter responderer ikke på follitropin alfa/hCG-behandling. Follitropin alfa skal ikke brukes når en effektiv respons ikke kan oppnås. Sædanalyse anbefales 4-6 måneder etter behandlingsstart for å hjelpe med å vurdere responsen. Hjelpestoffer: Preparatet inneholder <1 mmol natrium (23 mg)/dose, dvs. tilnærmet natriumfritt.Interaksjoner
Graviditet, amming og fertilitet
Bivirkninger
Overdosering/Forgiftning
Effekten av overdosering er ukjent, men det er en mulighet for at OHSS kan forekomme.Egenskaper og miljø
Pakninger, priser og refusjon
GONAL-f, INJEKSJONSVÆSKE, oppløsning i ferdigfylt penn:
| Styrke | Pakning Varenr. |
Refusjon | Pris (kr) | R.gr. |
|---|---|---|---|---|
| 300 IE/0,48 ml | 1 stk. (ferdigfylt penn) 141438 |
- |
1 117,90 | C |
GONAL-f, INJEKSJONSVÆSKE, oppløsning i ferdigfylt penn:
| Styrke | Pakning Varenr. |
Refusjon | Pris (kr) | R.gr. |
|---|---|---|---|---|
| 450 IE/0,72 ml | 1 stk. (ferdigfylt penn) 391010 |
- |
1 658,40 | C |
GONAL-f, INJEKSJONSVÆSKE, oppløsning i ferdigfylt penn:
| Styrke | Pakning Varenr. |
Refusjon | Pris (kr) | R.gr. |
|---|---|---|---|---|
| 900 IE/1,44 ml | 1 stk. (ferdigfylt penn) 389637 |
- |
3 263,70 | C |
SPC (preparatomtale)
GONAL-f INJEKSJONSVÆSKE, oppløsning i ferdigfylt penn 300 IE/0,48 ml GONAL-f INJEKSJONSVÆSKE, oppløsning i ferdigfylt penn 450 IE/0,72 ml GONAL-f INJEKSJONSVÆSKE, oppløsning i ferdigfylt penn 900 IE/1,44 ml |
06.01.2025
Sist endret: 25.02.2025
(priser og ev. refusjon oppdateres hver 14. dag)