Virkestoff: Buprenorfin
Pakningsvedlegg
PAKNINGSVEDLEGG :
Bupredine vet 0,3 mg/ml injeksjonsvæske, oppløsning til hund, katt og hest
1. NAVN OG ADRESSE PÅ INNEHAVER AV MARKEDSFØRINGSTILLATELSE SAMT PÅ TILVIRKER SOM ER ANSVARLIG FOR BATCHFRIGIVELSE, HVIS DE ER FORSKJELLIGE
Innehaver av markedsføringstillatelse:
Le Vet Beheer B.V.
Wilgenweg 7
3421 TV Oudewater
Nederland
Tilvirker ansvarlig for batchfrigivelse:
Produlab Pharma B.V.
Forellenweg 16
4941 SJ Raamsdonksveer
Nederland
2. VETERINÆRPREPARATETS NAVN
Bupredine vet 0,3 mg/ml injeksjonsvæske, oppløsning til hund, katt og hest
buprenorfin
3. DEKLARASJON AV VIRKESTOFF(ER) OG HJELPESTOFF(ER)
1 ml inneholder:
Virkestoff:
Buprenorfin (som hydroklorid) 0,3 mg
tilsvarende 0,324 mg buprenorfinhydroklorid
Hjelpestoffer:
Klorkresol 1,35 mg
Klar, fargeløs og vandig oppløsning.
4. INDIKASJON(ER)
Hund og katt: Postoperativ smertelindring.
Hest: Postoperativ smertelindring i kombinasjon med sedering.
Hund og hest: Forsterkning av de sedative effektene til sentraltvirkende midler.
5. KONTRAINDIKASJONER
Skal ikke tilføres intratekalt eller periduralt.
Skal ikke brukes preoperativt ved keisersnitt (se avsnittet om spesielle advarsler).
Skal ikke brukes ved kjent overfølsomhet overfor virkestoffet eller noen av hjelpestoffene.
6. BIVIRKNINGER
Sikling (salivering), langsom hjerterytme (bradykardi), lav kroppstemperatur (hypotermi), uro (agitasjon), uttørring (dehydrering) og liten pupill (miose) kan oppstå hos hund, og i sjeldne tilfeller forhøyet blodtrykk (hypertensjon) og rask hjerterytme (takykardi).
Det er vanlig at stor pupill (mydriasis) og tegn på eufori (overdreven maling, skritting, gniing) oppstår hos katter. Dette vil vanligvis opphøre innen 24 timer.
Hos hest kan bruk av buprenorfin, uten forutgående bruk av et sedativum, forårsake oppjaget tilstand (eksitasjon) og spontan bevegelsesaktivitet.
Buprenorfin kan i noen tilfeller forårsake åndedrettsdepresjon (se avsnittet om spesielle advarsler). Ved bruk som anvist sammen med sedativer eller beroligende midler hos hest, er eksitasjon minimal, men ustøhet (ataksi) kan noen ganger være markert.
Buprenorfin kan redusere mage-tarmbevegelser (gastrointestinal motilitet) hos hest, men kolikk er sjeldent rapportert.
Frekvensen av bivirkninger angis etter følgende kriterier:
Svært vanlige (flere enn 1 av 10 behandlede dyr får bivirkning(er))
Vanlige (flere enn 1 men færre enn 10 av 100 behandlede dyr)
Mindre vanlige (flere enn 1 men færre enn 10 av 1000 behandlede dyr)
Sjeldne (flere enn 1 men færre enn 10 av 10 000 behandlede dyr)
Svært sjeldne (færre enn 1 av 10 000 behandlede dyr, inkludert isolerte rapporter).
Hvis du legger merke til noen bivirkninger, også slike som ikke allerede er nevnt i dette pakningsvedlegget, eller du tror at legemidlet ikke har virket, bør dette meldes til din veterinær.
7. DYREARTER SOM PREPARATET ER BEREGNET TIL (MÅLARTER)
Hund, katt og hest.
8. DOSERING FOR HVER MÅLART, TILFØRSELSVEI(ER) OG TILFØRSELSMÅTE
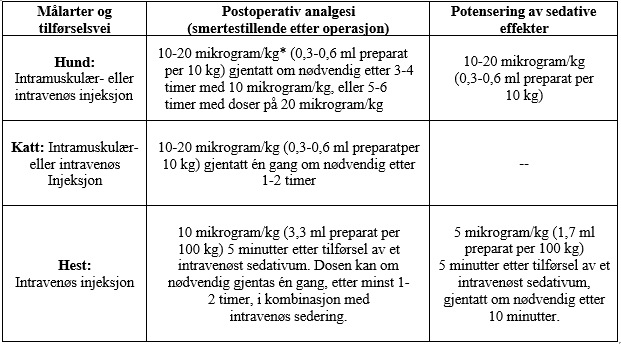
* Doseringene som er angitt i mikrogram/kg i tabellen over viser til buprenorfin (som hydroklorid). Kg i tabellen viser til kroppsvekt.
Ved bruk hos hest må et intravenøst sedativum gis innen fem minutter før injisering av buprenorfin.
Hos hund oppstår sedative effekter innen 15 minutter etter tilførsel. Det kan hende at smertestillende effekt ikke er fullt utviklet før etter 30 minutter. For å sikre smertestillende effekt under kirurgi og umiddelbart ved oppvåkning, skal veterinærpreparatet gis før operasjon som en del av premedisineringen.
Ved tilførsel for forsterkning av sedering eller som en del av premedisinering, skal dosen av andre sentraltvirkende midler, som acepromazin eller medetomidin, reduseres. Reduksjonen vil avhenge av graden av sedering som kreves, det individuelle dyret, typen av andre midler som er inkludert i premedisineringen samt hvordan anestesi skal innledes og opprettholdes. Det kan også være mulig å redusere mengden inhalasjonsanestesi som brukes.
9. OPPLYSNINGER OM KORREKT BRUK
Dyr som får opioider med beroligende og smertestillende egenskaper, kan ha varierende respons. Derfor bør responsen til de enkelte dyrene overvåkes, og påfølgende doser skal justeres tilsvarende.
I enkelte tilfeller kan det hende at gjentatte doser ikke gir ytterligere smertelindring. I slike tilfeller bør det vurderes å bruke egnet injiserbart NSAID.
En egnet gradert sprøyte skal brukes for å gi nøyaktig dosering.
Proppen skal ikke punkteres mer enn 100 ganger (med en 21G eller 23G nål).
10. TILBAKEHOLDELSESTID(ER)
Preparatet er ikke godkjent for hester til konsum.
11. SPESIELLE FORHOLDSREGLER VEDRØRENDE OPPBEVARING
Oppbevares utilgjengelig for barn.
Dette veterinærpreparatet krever ingen spesielle oppbevaringsbetingelser.
Bruk ikke dette veterinærpreparatet etter den utløpsdatoen som er angitt på esken og etiketten etter "EXP". Utløpsdatoen henviser til den siste dagen i den måneden.
Holdbarhet etter anbrudd av beholder: 28 dager
12. SPESIELLE ADVARSLER
Spesielle advarsler for de enkelte målarter:
Ettersom buprenorfin metaboliseres i leveren, kan intensiteten og varigheten av effekten påvirkes hos dyr med nedsatt leverfunksjon.
Spesielle forholdsregler for bruk til dyr:
Sikkerheten til buprenorfin har ikke vært demonstrert hos kattunger eller valper yngre enn 7 uker, eller hos hester yngre enn 10 måneder og som veier under 150 kg. Bruk hos slike dyr skal derfor baseres på nytte/risikovurdering gjort av veterinær.
Sikkerheten har ikke vært fullt evaluert hos klinisk kompromitterte katter og hester. Langtidssikkerhet av buprenorfin har ikke vært undersøkt utover 5 påfølgende dager med tilførsel hos katt eller 4 atskilte tilførslerr på tre påfølgende dager hos hest.
Effekten av et opioid på hodeskade avhenger av typen skade og skadens alvorlighetsgrad samt åndedrettsstøtte som gis. Ved nyre-, hjerte- eller leverdysfunksjon, eller sjokk, kan det være større risiko forbundet med bruk av veterinærpreparatet. I alle disse tilfellene skal veterinærpreparatet brukes i samsvar med nytte/risiko-vurdering gjort av behandlende veterinær.
Buprenorfin kan noen ganger gi åndedrettsdepresjon, og i likhet med andre opioide legemidler bør det utvises forsiktighet ved behandling av dyr med nedsatt åndedrettsfunksjon eller dyr som får legemidler som kan gi åndedrettsdepresjon.
Gjentatt tilførsel tidligere enn det anbefalte gjentakelsesintervallet som foreslås i avsnittet om dosering for hver målart, anbefales ikke.
Hos hest har bruk av opioider vært forbundet med eksitasjon, men effekten av buprenofrin er minimal ved bruk sammen med sedativer eller beroligende midler som detomidin, romifidin, xylazin og acepromazin.
Ataksi er en kjent effekt av detomidin og lignende stoffer. Derfor kan dette ses etter tilførsel av buprenorfin sammen med slike stoffer. I noen tilfeller kan ataksi være markert. For å sikre at ataktiske hester som er sedert med detomidin/buprenorfin ikke mister balansen, bør de ikke flyttes eller håndteres på annen måte som kan forringe hestens stabilitet.
Spesielle forholdsregler for personen som håndterer veterinærpreparatet:
Ettersom buprenorfin har opioidlignende effekt, bør det utvises forsiktighet for å unngå selvinjeksjon eller inntak.
Ved utilsiktet selvinjeksjon eller inntak, søk straks legehjelp og vis legen pakningsvedlegget eller etiketten.
Veterinærpreparatet kan foråsake hud- eller øyeirritasjon eller overfølsomhetsreaksjoner hvis det oppstår kontakt. Etter kontakt med øyne, hud eller munn, vask det berørte området grundig med vann. Oppsøk legehjelp ved overfølsomhetsreaksjoner eller hvis irritasjonen vedvarer. Vask hendene etter bruk.
Til legen:
Nalokson skal være tilgjengelig i tilfelle utilsiktet selvinjeksjon.
Drektighet og diegiving:
Drektighet: Laboratoriestudier i rotter har ikke vist teratogene effekter. Disse studiene har imidlertid vist tap av foster etter implantering samt tidlig fosterdød.
Ettersom det ikke er utført studier av reproduksjonstoksisitet hos målartene, skal veterinærpreparatet bare brukes i samsvar med nytte/risikovurdering gjort av behandlende veterinær.
Veterinærpreparatet skal ikke brukes preoperativt ved keisersnitt på grunn av risikoen for åndedrettsdepresjon hos avkommet i tilknytning til fødsel, og skal bare brukes postoperativt med særlig forsiktighet (se nedenfor).
Diegiving:
Studier av diegivende rotter har vist at, etter intramuskulær injeksjon av buprenorfin, var konsentrasjonen av uendret buprenorfin i melken lik eller høyere enn i plasma. Ettersom det er sannsynlig at buprenorfin skilles ut i morsmelk hos andre arter, er bruk under diegiving ikke anbefalt. Skal bare brukes i samsvar med nytte/risikovurdering gjort av behandlende veterinær.
Interaksjon med andre legemidler og andre former for interaksjon:
Buprenorfin kan forårsake noe døsighet, som kan forsterkes av andre sentraltvirkende midler, inkludert beroligende midler, sedativer og hypnotika.
Det er indikasjoner hos mennesker på at terapeutiske doser av buprenorfin ikke reduserer den smertestillende effekten av standarddoser av en opioidagonist, og at når buprenorfin brukes innenfor det normale terapeutiske området, kan standarddoser av opioidagonister gis før effektene av den første har opphørt, uten å gi redusert smertelindring. Det anbefales imidlertid at buprenorfin ikke brukes sammen med morfin eller andre smertestillende midler av opioidtypen, f.eks. etorfin, fentanyl, petidin, metadon, papaveretum eller butorfanol.
Buprenorfin har vært brukt sammen med acepromazin, alfaksalon/alfadalon, atropin, detomidin, deksmedetomidin, halotan, isofluran, ketamin, medetomidin, propofol, romifidin, sevofluran, tiopenton og xylazin.
Ved bruk sammen med sedativer kan depressive effekter på hjertefrekvens og åndedrett økes.
Overdosering (symptomer, førstehjelp, antidoter):
Ved overdosering skal støttende tiltak iverksettes og, hvis egnet, kan nalokson eller åndedrettsstimulerende midler brukes.
Ved overdosering hos hund kan buprenorfin forårsake apati (letargi). Ved svært høye doser kan det observeres langsom hjerterytme (bradykardi) og liten pupill (miose).
Studier på hest der buprenorfin har vært gitt sammen med sedativer, har vist svært få bivirkninger ved opptil fem ganger den anbefalte dosen, men ved bruk alene kan det forårsake eksitasjon.
Ved bruk for å gi smertelindring hos hest, er sedering sjelden sett, men det kan oppstå ved dosenivåer over de anbefalte nivåene.
Nalokson kan være fordelaktig for å reversere redusert åndedrettsfrekvens.
I toksikologiske studier av buprenorfinhydroklorid hos hund ble gallegangshyperplasi observert etter peroral tilførsel i ett år med dosenivåer på 3,5 mg/kg/dag og over. Gallegangshyperplasi ble ikke observert etter daglig intramuskulær injeksjon av dosenivåer opptil 2,5 mg/kg/dag i 3 måneder. Dette er godt over ethvert klinisk doseregime hos hund.
Se også avsnittet om spesielle forholdsregler for bruk til dyr og avsnittet om bivirkninger, i dette pakningsvedlegget.
Uforlikeligheter:
Da det ikke foreligger forlikelighetsstudier, bør dette veterinærpreparatet ikke blandes med andre veterinærpreparater.
13. SÆRLIGE FORHOLDSREGLER FOR HÅNDTERING AV UBRUKT LEGEMIDDEL, RESTER OG EMBALLASJE
Ubrukt legemiddel, legemiddelrester og avfall skal kasseres i overensstemmelse med lokale krav.
14. DATO FOR SIST GODKJENTE PAKNINGSVEDLEGG
13.12.2021
15. YTTERLIGERE INFORMASJON
Pakningsstørrelser: 5 ml, 10 ml, 20 ml, 50 ml og 100 ml.
Ikke alle pakningsstørrelser vil nødvendigvis bli markedsført.
For ytterligere opplysninger om dette veterinærpreparatet, ta kontakt med lokal representant for innehaver av markedsføringstillatelsen.