FELLESKATALOGEN
INJEKSJONSVÆSKE, oppløsning i ferdigfylt penn 120 mg: Hver ferdigfylte penn inneh.: Galkanezumab 120 mg, L-histidin, L-histidinhydrokloridmonohydrat, polysorbat 80, natriumklorid, vann til injeksjonsvæsker.
Dosering
Mht. sporbarhet skal preparatnavn og batchnr. noteres i pasientjournalen. Behandling bør initieres av lege med erfaring i diagnostisering og behandling av migrene.
Voksne, inkl. eldre >65 år
Anbefalt dose: 240 mg (2 injeksjoner à 120 mg) som innledende bolusdose, deretter 120 mg 1 gang pr. måned. Behandlingsnytte bør vurderes innen 3 måneder etter behandlingsoppstart. Ytterligere beslutning om å fortsette behandlingen bør gjøres individuelt. Evaluer deretter behovet for å fortsette behandlingen regelmessig.
Glemt dose Pasienten bør rådes til å injisere glemt dose så snart som mulig, og deretter fortsette med dosering 1 gang pr. måned.
Spesielle pasientgrupper
- Nedsatt lever-/nyrefunksjon: Dosejustering ikke nødvendig ved lett til moderat nedsatt lever- eller nyrefunksjon.
- Barn og ungdom: 6-18 år: Sikkerhet og effekt ikke fastslått, ingen data. <6 år: Bruk er ikke relevant.
Tilberedning/Håndtering Se pakningsvedlegget. Til engangsbruk. Skal ikke ristes. For en mer behagelig injeksjon, la pennen ligge ute i romtemperatur i 30 minutter før injeksjon. Skal ikke varmes opp ved bruk av varmekilder som varmt vann eller mikrobølgeovn. Bør beskyttes mot direkte sollys. Sjekkes visuelt før bruk. Skal ikke injiseres hvis den er uklar, misfarget eller har små partikler.
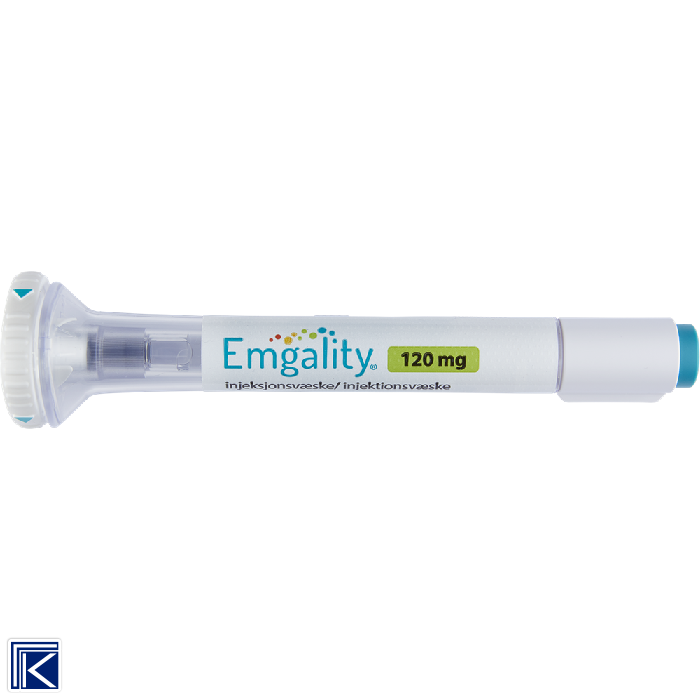
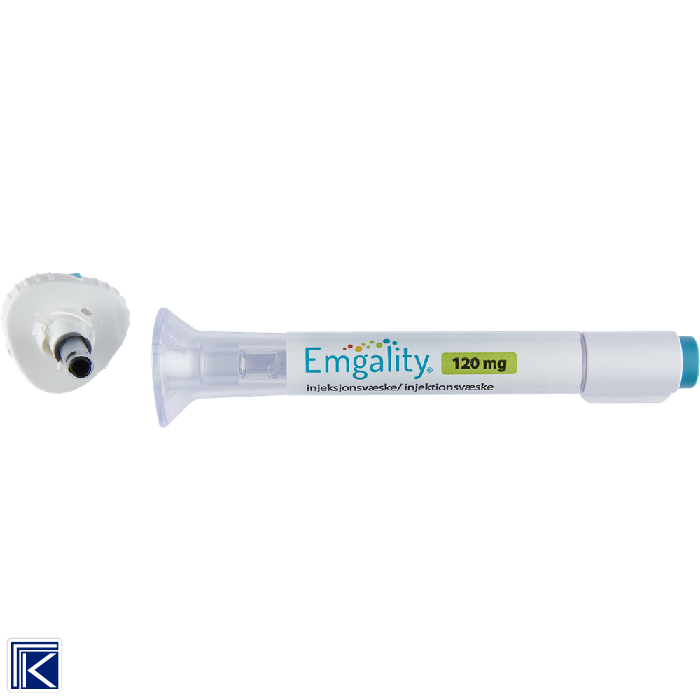
Administrering Hele innholdet skal injiseres s.c. i magen, låret, baksiden av overarmen eller i seteområdet, se pakningsvedlegget. Injeksjonsstedene skal byttes på, og skal ikke settes i områder hvor huden er øm, har blåmerker, er rød eller hard. Etter opplæring kan pasienten selv administrere ved å følge bruksanvisningen, dersom helsepersonell vurderer det som hensiktsmessig.
Forsiktighetsregler
Hjerte/kar: Ingen sikkerhetsdata ved alvorlige kardiovaskulære sykdommer, se SPC for ytterligere informasjon. Alvorlig overfølsomhet: Alvorlige overfølsomhetsreaksjoner, inkl. tilfeller av anafylaksi, angioødem og urtikaria, er rapportert. Alvorlige overfølsomhetsreaksjoner kan oppstå i løpet av 1. døgn etter administrering, men tilfeller med forsinket debut (fra >1 dag til 4 uker etter administrering) er også rapportert. I noen tilfeller varte overfølsomhetsreaksjoner over lengre tid. Ved alvorlig overfølsomhetsreaksjon bør administreringen avbrytes umiddelbart og egnet behandling igangsettes. Pasienter bør informeres om muligheten for forsinket overfølsomhetsreaksjon og instrueres om å kontakte lege. Hjelpestoffer: Inneholder <1 mmol (23 mg) natrium pr. dose, og er så godt som natriumfritt. Bilkjøring og bruk av maskiner: Liten påvirkning forventes på evnen til å kjøre bil eller bruke maskiner. Vertigo er rapportert ved behandling.Graviditet, amming og fertilitet
GraviditetBegrensede data. Dyrestudier viser ingen direkte eller indirekte skadelige reproduksjonseffekter. Humant immunglobulin (IgG) krysser placentabarrieren. Som et forsiktighetstiltak bør bruk under graviditet unngås.
AmmingOvergang i morsmelk er ukjent. Humant IgG utskilles i morsmelk de første dagene etter fødsel, og avtar til lave konsentrasjoner etter kort tid. Risiko for diende spedbarn kan derfor ikke utelukkes i denne korte perioden. Bruk under amming kan deretter vurderes, kun dersom klinisk nødvendig.
FertilitetDyrestudier indikerer ingen skadelige effekter mht. fertilitet.
Bivirkninger
Frekvensintervaller: Svært vanlige (≥1/10), vanlige (≥1/100 til <1/10), mindre vanlige (≥1/1000 til <1/100), sjeldne (≥1/10 000 til <1/1000), svært sjeldne (<1/10 000) og ukjent frekvens.
Overdosering/Forgiftning
BehandlingOvervåk for ev. tegn/symptomer på bivirkninger. Symptomatisk behandling igangsettes umiddelbart.
Egenskaper og miljø
KlassifiseringHumanisert monoklonalt antistoff (IgG4).
VirkningsmekanismeBindes til kalsitonin-genrelatert peptid (CGRP) med høy affinitet og høy spesifisitet, og hindrer CGRPs virkning på CGRP-reseptorer.
AbsorpsjonCmax nås 5 dager etter bolusdose 240 mg.
FordelingVd 7,3 liter.
Halveringstid27 dager.
Pakninger, priser og refusjon
Emgality, INJEKSJONSVÆSKE, oppløsning i ferdigfylt penn:
| Styrke | Pakning Varenr. |
Refusjon | Pris (kr) | R.gr. |
|---|---|---|---|---|
| 120 mg | 1 stk. (ferdigfylt penn) 468840 |
- |
5 107,50 | C |
Individuell stønad
Galkanezumab
Legemidler: Emgality injeksjonsvæske
Indikasjon: Forebyggende behandling av kronisk migrene.
For blåreseptsøknad og -vedtak, se Tjenesteportal for helseaktører
Basert på SPC godkjent av DMP/EMA:
12.01.2026
Sist endret: 21.06.2022
(priser og ev. refusjon oppdateres hver 14. dag)